- Wasserstoff
- Stickstoff
- Sauerstoff
- Kohlenstoffdioxid
- unbekannte Kohlenwasserstoffverbindung CxHy
Der Dreiwegehahn wird nach dem Füllen so gestellt, dass das jeweilige Gas durch die Düse ausströmen kann. Man misst die Zeit, die das Volumen von 100 mL des Gases zum Ausströmen braucht.
Zur Auswertung kann man nun die Ausströmungszeiten gegen die Molaren Massen der Gase auftragen. Aus der erhaltenen Kurve lässt sich über die Ausströmungszeit die Molare Masse des unbekannten Gases ablesen.
Die Molare Masse des unbekannten Gases lässt sich auch über folgende Beziehung (Grahamsche Gesetz, 1829), die man über die erhaltenen Werte (siehe Tabelle) herleiten kann, berechnen:
M1 / M2 = t12 / t22
M(CxHy) = M (N2)
* (9,0)2 / (8,8)2 = 28 g / mol *
1,046
M(CxHy) = 29,3 g /
mol
Bei dem Gas könnte es sich um Ethan (M = 30 g / mol) handeln.
Beispiel:
| Gas | Molare Masse g / mol |
Ausströmungszeit s |
| H2 | 2 | 2,4 |
| N2 | 28 | 8,8 |
| O2 | 32 | 9,2 |
| CO2 | 44 | 11,1 |
| CxHy | 9,0 |
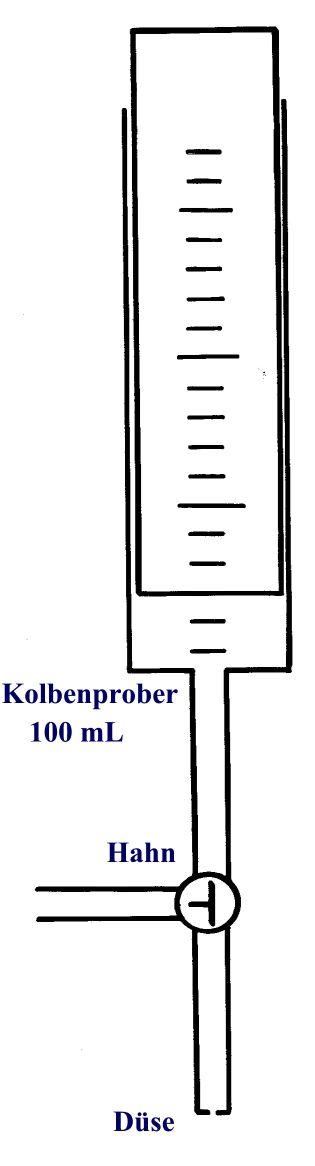
Zur Herstellung der Düse klebt man an ein Glasrohr des Dreiwegehahns eine dünne Pappscheibe, die mittig ein kleines Loch hat.